Китайські вчені розробили унікальні нанокапсули для неінвазивної доставки в мозок і націлювання на пухлинні клітини ліків. На мишах вони продемонстрували ефективну та безпечну стратегію генної терапії гліобластоми — найбільш розповсюдженої агресивної форми пухлин мозку. Про те, як вдалося обійти гематоенцефалічний бар'єр і поцілити точно в пухлину, повідомили в журналі Science Advances.
Зображення мультиформної гліобластоми людини – злоякісної пухлини мозку. Sbrandner / Wikimedia Commons
Що таке гематоенцефалічний бар'єр і як він заважає при лікуванні?
Однією з перепон для лікування гліобластоми є гематоенцефалічний бар'єр (ГЕБ) – захисний механізм, що вберігає мозок від потрапляння з крові небажаних речовин та мікроорганізмів, а також протиракових препаратів. Одним із методів обійти його є пряма ін'єкція ліків у тканину мозку, але це несе загрозу її пошкодження. Іншим способом є доставлення до тканин системи редагування генів CRISPR/Cas9 вірусними векторами (лентовірусами та аденоасоційованими вірусами), які вводяться у кровотік. CRISPR/Cas9 є інструментом додавання, видалення або зміни генетичного матеріалу всередині клітин. Ця технологія має великі перспективи для лікування деяких захворювань. Це доволі точний метод редагування генів, але наразі він не підходить для використання у мозку через занепокоєння стосовно підвищення ризику небажаних генетичних мутацій та імуногенності. Крім того, метод складно масштабувати до серійного виробництва. З іншого боку, наявні невірусні системи доставки обмежені через низьку ефективність навантаження, погане націлення і ризики нейрозапалення. Також ці методи серйозно обмежені в проникненні крізь ГЕБ. Тому важливо розробити безпечне й ефективне неінвазивне доставлення комплексів CRISPR/Cas9, яке б могло подолати ГЕБ. Дослідники Об'єднаного центру біомедичних інновацій Унівеситетів Хенань та Макуорі розробили нову платформу доставки системи CRISPR/Cas9, яка задовольняє цим критеріям.
Як вдалося розв'язати проблему проходження ГЕБ?
Вчені розробили крихітні біорозкладні нанокапсули розміром усього 30 нанометрів, що дозволяє їм легко проходити через бар'єр. Нанокапсули складаються з полімерної нетоксичної оболонки із майже нейтральним поверхневим зарядом. Це захищає вантаж від деградації та сприяє його стабільності в крові, забезпечуючи цілісність протягом тривалої подорожі кровотоком на шляху до мозку. Капсулу майже на 100 відсотків можна навантажити лікарським засобом, який вивільняється при досягненні пухлини. Цього разу використали систему CRISPR/Cas9, націлену на ген PLK1, який відіграє ключову роль у розвитку нових клітин і надмірно експресується при гліобластомі.
Які результати показали нанокапсули?
Здатність нанокапсул перетинати ГЕБ оцінили на мишах із гліобластомою, що отримали внутрішньовенну ін'єкцію. Результати показали, що у тварин, яким дали розроблені нанокапсули, пригнітився ріст пухлини без помітного зниження маси тіла, і вони в середньому жили 68 днів. Натомість миші контрольних груп, яким давали нанокапсули не націлені на конкретний ген або фізіологічний розчин, швидко втрачали вагу внаслідок швидкої проліферації пухлин і прожили лише 24 дні або менше. Важливо, що лікування не спричинило серйозних побічних ефектів, утім, дослідники помітили незначне ураження генів у ділянках пухлинної тканини з частотою мутацій нижче 0,5 відсотка.
Надалі вчені збираються поліпшити нанокапсули з огляду на те, що пухлини мозку мають складний патогенез і редагування одного гена навряд чи зможе повністю знищити пухлину. Тому наступним кроком буде націлення на декілька генів для досягнення більш ефективного лікування пухлини мозку.
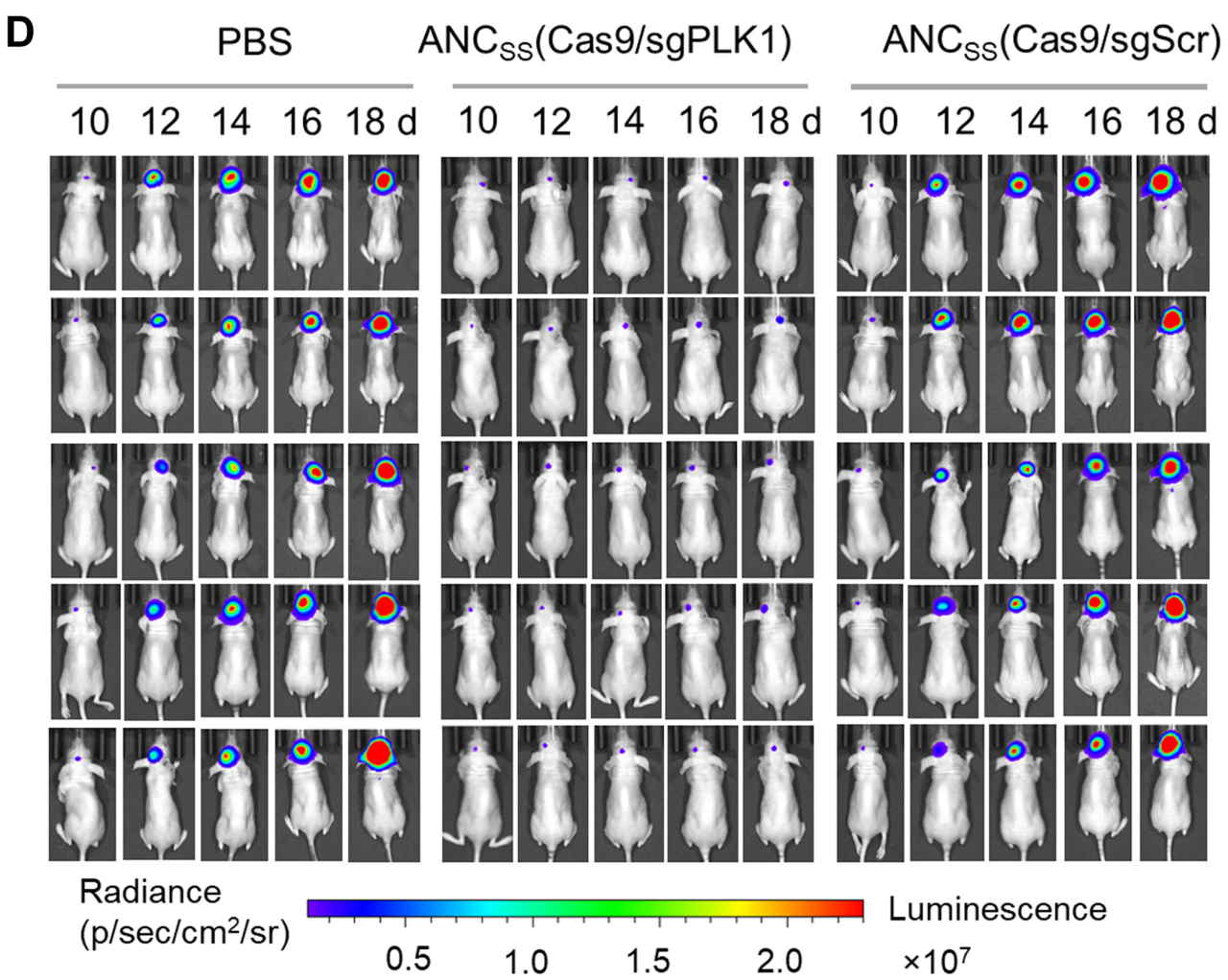
Ефективність редагування геному нанокапсулою CRISPR-Cas9 у мишей протягом 18 днів нагляду, де зниження інтенсивності сигналу біолюмінесценції свідчить про значне пригнічення росту пухлини. Ліворуч: після отримання нанокапсули з фізіологічним розчином. Посередині: ті, хто отримав нанокапсули з геном PLK1. Праворуч: ті, хто отримав нанокапсули не націлені на конкретний ген.





